32. Összefoglalás
25. Kémiai reakciók:
- Hypo és sósav rakciója
- Reakciók csoportosítása: (az ugye megvan, hogy a halmazállapotváltozás, oldódás, kristályosodás, mágneses szétválasztás, desztillálás - ezek nem kémiai reakciók, hanem FIZIKAI VÁLTOZÁSOK)
- Időbeli lefolyás szerint: gyors - mérhető idejű - lassú
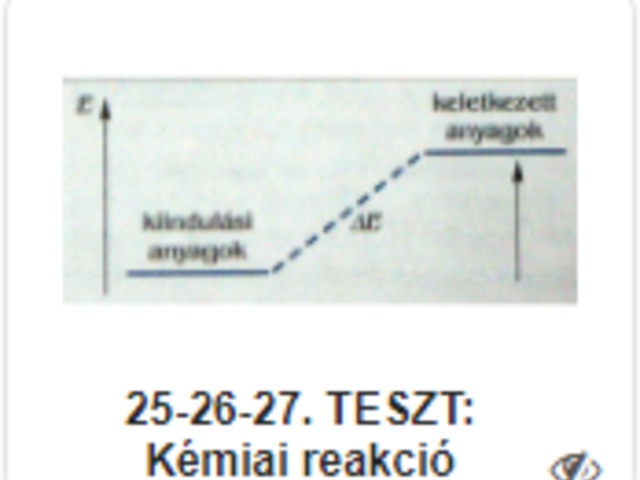
- Energiaváltozás szerint: exoterm (egyesülés) - endoterm (bomlás)
- Részecskeszám változás szerint: egyesülés - bomlás
- Részecskeátmenet szerint: elektronátmenettel járó (redoxi) - protonátmenettel járó (sav-bázis) reakció
- QUIZIZZ
26. Kémiai egyenlet
Quizlet
- Ezt a 12 egyenletet kellene tudnod (Mf. 25-26. leckéje alapján!), gyakorolhatsz QUIZLETBEN! Meg tudod dönteni a szintidőt? 18 sec! Ha megdöntöd, jobb vagy nálam! (vagy legalább is gyorsabb)
27. Kémiai számítsok
Ha megírod 80% fölé --> jár az ötös! Csak lépj be LearnApp fiókodba, és ott oldd meg! (25-26-27. TESZT: kémiai reakciók)

28. Oxidáció és redukció
Oxidáció:
- Oxigén felvételt vagy elektron leadást jelent
- Oxidálószer lehet az oxigén és a körülötte lévő nemfémek (kén, halogének, esetleg nitrogén)
Redukció:
- Oxigén leadást vagy elektron felvételt jelent
- Redukálószer lehet az hidrogén és a fémek (különösen jó redukálószerek az I. és a II. főcsoport)
Itt sok-sok egyenletet írtunk megint! (28. Redoxi TESZT)
30. Savak
Sav-bázis elméleteket (Arhenius, Brönsted)
Tudd: sósavszökőkút
Dolgozatban:
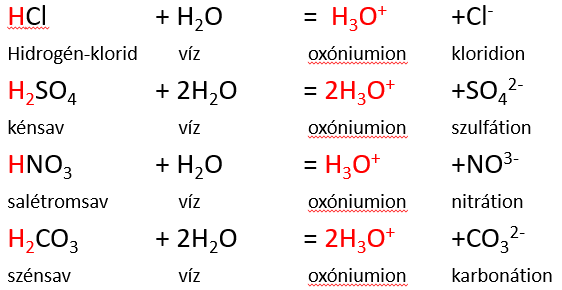
- Írd fel adott sav képletét és a savmaradék nevét és képletét! (sósav, kénsav, salétromsav, szénsav, foszforsav)
- Írd fel adott sav reakcióját vízzel,
- Nevezd el a termékeket!
- Hány értékű a sav? (a válasz: amennyi H van benne, tehát 1 v. 2)
- Milyen kémhatású a vizes oldata? (savas)
- Milyen színű benne az adott indikátor? (lakmusz - piros, fenolftalein - színtelen, univerzál - piros)
- Mekkora a pH-ja? (0-7 közti, vagy 7-nél kisebb)
Reakciót felírni kétféleképpen lehet:
Arhenius: a savak disszociálnak:

Brönsted: a hidrogéniont felveszi egy víz, és oxóniumion keletkezik
31. Bázisok
Ammónia, NaOH, KOH, Ca(OH)2 reakciója vízzel
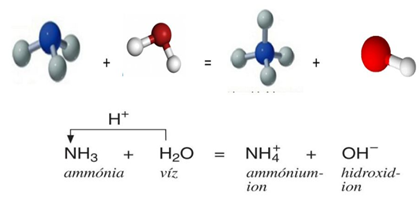
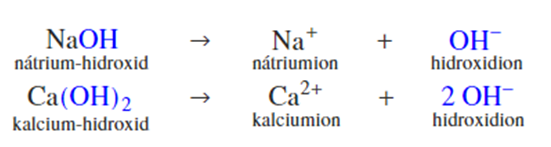
- Nevezd el a termékeket!
- Hány értékű a bázis? (a válasz: amennyi OH-t ad, tehát 1 v. 2)
- Milyen kémhatású a vizes oldata? (lúgos)
- Milyen színű benne az adott indikátor? (lakmusz - kék, fenolftalein - piros, univerzál - kék v. zöld)
- Mekkora a pH-ja? (7-14 közti, vagy 7-nél nagyobb)
32. Közömbösítés

Sav-bázis reakciók - teszt
Dolgozatban:
1.Egy kísérlet értelmezése (hypo és sósav reakciója, sósvszökőkút, ammónia szökőkút
2.Írd fel az adott redoxi egyenletet, rendezd! (Ezeket kell tudni)
- Állapítsd meg mi oxidálódik - redukálódik, mi az oxidálószer - redukálószer!
- Jellemezd a reakciót: egyesülés vagy bomlás, exoterm vagy endoterm
3.Lesz egy számolás (ilyen típusú: 27g alumíniumból hány g alumínium-oxidot lehet előállítani? Egyenletet is írj!)
4.Egy sav vagy bázis reakcióegyenlet írása, jellemzése (ld. fent)
5.Savak és bázisok képlete, neve, savmaradék neve
6.Egy közömbösítés
7.Teszt: a fenti LearnApp kérdésekből összeválogatva)